




Dieser Hypertext fasst unserer Buchseiten 106-114 zusammen.
Klickt man im Inhaltsverzeichnis auf die blauen Pfeile, so springt man innerhalb des Textes nach unten in das entsprechende Kapitel. Mit einem Klick auf die Kapitelüberschrift springt man vom Inhaltsverzeichnis direkt in ein ausführlicheres Kapitel eines anderen Textes.
 |
die Zelle als offenes System im Fließgleichgewicht - Seiten 116-117 |
|---|---|
 |
Zellatmung und Gärung - Seiten 118-119 |
 |
Glykolyse - Seiten 120-121 |
 |
Oxidative Decarboxylierung und Zitratzyklus - Seiten 122-123 |
 |
Die folgenden Abschnitte fassen zusammen, was die Seiten 116-121 unseres Zellbiologie-Schulbuches zum Thema Stoffwechsel vermitteln. Meine Zusammenfassungen dieser Seiten sollen aber nur als Beispiel und der Kontrolle dienen. Damit man sich nicht um eine wichtige Gelegenheit zur Übung selbständigen Denkens, Analysierens und Formulieres bringt, sollte man vor meinen Zusammfassungen die Buchseiten selber lesen und versuchen, wesentliche Informationen in eigenen Worten so knapp wie möglich und so ausführlich wie nötig zusammenzufassen. Das Werkzeug dafür hat jeder gesunde Mensch in seinem Gehirn. Eine weitere Möglichkeit aktiver Erarbeitung dieser Inhalte bieten klausurähnliche Aufgaben.
die Zelle als offenes System im Fließgleichgewicht - Seiten 116-117
|
|---|
Mit folgendem Link findet Du klausurähnliche Aufgaben zu den Buchseiten 116-117.
Lebende tierische und pilzliche Zellen müssen Stoffe aufnehmen, um aus diesen Energie oder Baustoffe für Wachstum oder Erneuerung zu gewinnen. Pflanzliche Zellen gewinnen ihre chemische Energie durch Umwandlung von Strahlungsenergie. Überhaupt keinen Stoffwechsel haben die Zellen in flüssigem Stickstoff gelagerter menschlicher Embryonen und anderer Lebewesen, die gerade eine Pause vom Leben machen.
Glucose ist ein Grundbaustein der in menschlichen Zellen nur zur Energiegewinnung genutzten Kohlenhydrate. Aminosäuren sind die Grundbausteine der Proteine, die der menschliche Organismus nur im Notfall zur Energiegewinnung nutzt. Wir zerlegen pflanzliche, pilzliche und tierische Proteine in Aminosäuren, um dann daraus unsere eigenen Proteine zu synthetisieren.
Komplexität ist eine Form von Ordnung. Ohne den ordnenden Einfluss der Lebewesen nimmt aber in der unbelebten Natur immer die Unordnung (Entropie) zu. Lebewesen müssen Energie aufwenden, um auf Kosten zunehmender Entropie in ihrer Umwelt die Ordnung im Inneren ihrer Zellen immer wieder zu erneuern, indem sie ständig neue Biomoleküle synthetisieren und größere Strukturen wie Membranen und Protein-Komplexe aufbauen.
Lebende Zellen und andere offene Systeme zeichnen sich dadurch aus, dass sie ständig Energie und Stoffe mit ihren Umgebungen austauschen. Zellen tun das in Form von Fließgleichgewichten, weil sie ungefähr ebenso viel Energie und Materie abgeben, wie sie im selben Zeitraum aufnehmen.
Fotosynthese nennt man den Lebensprozess, in dem pflanzliche Zellen Strahlungsenergie nutzen, um aus Wasser (H2O) und Kohlenstoffdioxid (CO2) Glucose (C6H12O6) und Sauerstoff (O2) zu produzieren.
Energie kann weder erschaffen noch vernichtet werden. (Es wird immer nur eine Energieform in eine andere umgewandelt. Dabei entsteht immer auch Wärmeenergie, die dann oft nicht mehr nutzbar ist. Deshalb verlieren Zellen für sie nutzbare Energie, wenn sie durch energetisch nicht begünstigte (endergone) chemische Reaktionen die Ordnung vergrößern (lokal die Entropie reduzieren), indem sie Aminosäuren mit Peptidbindungen zu Proteinen verknüpfen. Die Wärme wird an die Umwelt abgegeben, wo sie die Unordnung (Entropie) vergrößert. Darum müssen lebende Zellen ihren Energieverlust ständig durch die Aufnahme von Energie aus der Umwelt ausgleichen.)
Die Ordnung vergrößernde chemische Reaktionen laufen nur endergon und nicht spontan ab, weil sich nach dem zweiten Hauptsatz der Thermodynamik thermodynamische Systeme spontan nur in Richtung größerer Unordnung (Entropie) entwickeln.
Zellatmung und Gärung - Seiten 118-119
|
|---|
Mit folgendem Link findet Du klausurähnliche Aufgaben zu den Buchseiten 118-119.
Äußere Atmung heißt die Aufnahme von Sauerstoff mit Hilfe der Lunge und des Blutkreislaufes. Sie dient der Versorgung unserer Zellen mit Sauerstoff für die Kette chemischer Reaktionen der innere Atmung. Die äußere Atmung dient außerdem der Entsorgung des bei der Zellatmung entstehenden Kohlenstoffdioxids (CO2) durch Blutkreislauf und Lunge.
Bei der Verbrennung (vollständigen Oxidation mit Sauerstoff) in einem Kalorimeter sind die energiereiche Glucose und Sauerstoff die Edukte sowie Kohlenstoffdioxid und Wasser die energiearmen und deshalb sehr stabilen Produkte. Vor der Oxidation haben die wenig elektronegativen Kohlenstoff- und Wasserstoff-Atome größere Anteile an ihren Bindungselektronenpaaren. Nach der Oxidation ziehen die Sauerstoff-Atome aufgrund ihrer großen Elektronegativität die Bindungselektronenpaare stärker zu sich hin und verursachen positivere Ladungen an den Kohlenstoff- und Wasserstoff-Atomen. In diesem Zustand nennt man die Kohlenstoff- und Wasserstoff-Atome oxidiert.
In Zellen erfolgt der Abbau (die Oxidation) der Glucose in zahlreichen Teilschritten und die chemische Energie wird in kleinen Portionen freigesetzt.
Unser Buch unterteilt den Abbau der Glucose in unseren Zellen in drei Abschnitte: die Glykolyse, den Zitronensäurezyklus und die Atmungskette. Seine Autoren vergessen dabei allerdings die oxidative Decarboxylierung der Brenztraubensäure.
Leber- und Muskelzellen haben einen relativ hohen Energiebedarf. Deshalb brauchen sie besonders viele Mitochondrien, die als Kraftwerke der Zellen gelten, weil in ihnen die wichtigsten Schritte des Glucose-Abbaus und der damit verbundenen Produktion von ATP stattfinden.
In der Glykolyse finden zwei verschiedene energetische Kopplungen statt, bei denen jeweils ein ATP-Molekül den Energietransport von einer chemische Energie liefernden zu einer chemische Energie benötigenden chemischen Reaktion übernimmt. Die chemische Energie liefernden chemischen Reaktionen in der zweiten Hälfte der Glykolyse sind:
Die chemische Energie verbrauchenden und deshalb nur mit Hilfe des energiereichen ATP möglichen chemischen Reaktionen in der ersten Hälfte der Glykolyse sind:
Die energetischen Kopplungen funktionieren so, dass im ersten Schritt katalysiert durch die Enzyme Phosphoglycerinsäurekinase und Brenztraubensäurekinase jeweils ein Phosphatrest und mit ihm die energiereiche Atombindung von den energiereichen Substraten Glycerinsäure-1,3-bisphosphat und Phosphoenolbrenztraubensäure auf ADP übertragen werden, um energiereiches ATP zu bilden. Anschließend wird jeweils in einem zweiten Schritt durch die Enzyme Hexokinase bzw. Phosphofructokinase der Phosphatrest mit der energiereiche Atombindung von ATP auf die energieärmeren Substrate Glucose bzw. Fruchtose-6-Phosphat übertragen. Diese beiden Aktivierungsschritte liefern den Produkten Glucose-6-phosphat und Fructose-1,6-bisphosphat die chemische Energie für die jeweils folgenden chemischen Reaktionen.
|
Glykolyse nennt man in der Biochemie einen zentralen Stoffwechselweg im Energiestoffwechsel und den zentralen Prozess beim Abbau aller Kohlenhydrate in allen Eukaryoten. Selbst unter Bakterien und Archaeen ist die Glykolyse weit verbreitet. In 10 hintereinander geschalteten Stoffwechselreaktionen wird das Monosaccharid Traubenzucker (Glucose) zur doppelten Anzahl von Pyruvat-Molekülen abgebaut. Dabei werden insgesamt jeweils 2 Moleküle ATP und NADH gewonnen.
Vertiefende Informationen über die Glykolyse findet man auf einer Seite der Uni Düsseldorf. |
|
| Diese Darstellung der Glykolyse habe ich auf der Grundlage eines anonym unter der Lizenz Creative Commons Attribution-Share Alike 3.0 der Wikimedia Commons zur Verfügung gestellten Schemas erstellt, um meine Schüler nicht mit anderen Namen zu verwirren und um ein im ursprünglichen Schema fehlendes Detail zu ergänzen. | |
Glykolyse - Seiten 120-121
|
|---|
Mit folgendem Link findet Du klausurähnliche Aufgaben zu den Buchseiten 120-121.
Ausdauersportler benötigen für ihren Sport hauptsächlich Kohlenhydrate, weil sie während der Ausübung ihrer Sportarten viel Energie verbrauchen, anschließend jedoch kaum Muskeln aufbauen. Mit der Zuführung reiner Glucose sollten Ausdauersportler jedoch vorsichtig sein, weil zu hohe Glucose-Konzentrationen im Blut den Blutgefäßen schaden und deshalb die Ausschüttung größerer Mengen Insulin provozieren, wodurch als überschießende Reaktion die Konzentration der Glucose im Blut sogar unter das Normalniveau fallen und die Leistungsfähigkeit reduzieren kann.
Kraftsportler brauchen besonders viel Eiweiß bzw. Aminosäuren, weil Muskeln nach kurzen, intensiven Belastungen bis zur völligen Erschöpfung Aminosäuren für den Aufbau neuer Proteine brauchen, um sich durch Wachstum an langsam zunehmende Anforderungen anzupassen.
Die Glykolyse findet im Cytoplasma einer Zelle statt. Zehn unterschiedliche, zu einem Stoffwechselweg hintereinander geschaltetete Enzyme katalysieren die chemischen Reaktionen, durch welche ein Glucose-Molekül zu zwei Molekülen Brenztraubensäure im Gleichgewicht mit ihrem Anion Pyruvat abgebaut wird.
Das erste Substrat des Stoffwechselweges Glykolyse wird durch das Enzym Hexokinase praktisch irreversibel phosphoryliert, sodass als energiereicheres Produkt Glucose-6-phosphat entsteht. Die dafür erforderliche Energie wird durch eine energetische Kopplung aufgebracht, indem gleichzeitig das energiereiche Adenosintriphosphat zu ADP und Phosphat gespalten und die Phosphatgruppe auf die Glucose übertragen wird. Das Produktion D-Glucose-6-Phosphat hemmt die Aktivität der Hexokinase und damit seine eigene Produktion.
Die als erstes Enzym der Glykolyse aktive Hexokinase phosphoryliert nicht nur Glucose, sondern verschiedene Einfachzucker (Monosaccharide) wie Mannose und Fructose, die ebenfalls aus 6 C-Atomen bestehen. Die Hexokinasen der Säugetiere phosphorylieren auch sowohl die α- als auch die β-Form der Glucose. Sie besitzt aber eine größere Affinität zur α-D-Glucose. Dafür ist die Konzentration der β-D-Glucose im Gleichgewicht wässriger Lösungen etwa doppelt so groß. Das folgende Schema zeigt es nicht, aber das eigentliche Substrat der Hexokinase ist nicht ATP, sondern ATP2- verbunden mit Mg2+ oder Mn2+.
Das Enzym Phosphoglucoseisomerase wandelt Glucose-6-phosphat reversibel zu Fructose-6-phosphat um. Das bedeutet, dass die Phosphoglucose-Isomerase spezifisch für beide Substrate Glucose-6-phosphat und Fructose-6-phosphat ist. Meine alten Biochemie-Lehrbücher stellen die chemische Reaktion mal mit den α- und mal mit den β-D-Formen von Glucose-6-phosphat und Fructose-6-phosphat dar. Die Phosphoglucose-Isomerase scheint also zwischen beiden Formen nicht zu unterscheiden.
Anschließend erfolgt der zweite Aktivierungsschritt: Das Enzym Phosphofructokinase katalysiert die zweite energetische Kopplung, in welcher die Phosphatgruppe von Adenosintriphosphat auf das Substrat Fructose-6-phosphat übertragen wird und das Produkt Fructose-1,6-bisphosphat entsteht.
Im vierten Schritt der Glykolyse spaltet das Enzym Fructose-bisphosphat-Aldolase die D-Fructose-1,6-bisphosphat reversibel in die beiden Moleküle D-Glycerinaldehyd-3-phosphat und Dihydroxyaceton-phosphat.
Im fünften Schritt der Glykolyse wandelt das Enzym Triosephosphat-Isomerase Dihydroxyacetonphosphat reversibel in Glycerinaldehyd-3-phosphat um.
Im sechsten Schritt der Glykolyse wandelt das Enzym Glycerinaldehyd-3-phosphatdehydrogenase praktisch irreversibel Glycerinaldehyd-3-phosphat in Glycerinsäure-1,3-bisphosphat um und reduziert dabei NAD+ zu NADH. Die durch das Enzym Glycerinaldehyd-3-phosphatdehydrogenase katalysierte stark exotherme Oxidation der Aldehydgruppe des Substrates Glycerinaldehyd-3-phosphat zur Carboxylgruppe des Produktes Glycerinsäure-1,3-bisphosphat ermöglicht durch energetische Kopplung die Phosphorylierung der Carboxygruppe durch anorganisches Phosphat sowie die Reduzierung von NAD+ zu NADH+H+.
Das verglichen mit NAD+ reduzierte und energiereichere NADH aus der Glykolyse dient in der Atmungskette als energielieferndes Coenzym bei der Synthese von ATP. Im folgenden siebten Schritt der Glykolyse überträgt das Enzym Phosphoglyceratkinase eine Phosphatgruppe von Glycerinsäure-1,3-bisphosphat auf ADP und umgekehrt (reversibel) von ATP auf Glycerinsäure-3-phosphat.
Der achte Schritt der Glykolyse ist die reversible Umlagerung der Phosphatgruppe vom dritten C-Atom von Glycerinsäure-3-phosphat zum zweiten C-Atom von Glycerinsäure-2-phosphat durch das Enzym Phosphoglyceratmutase.
Der neunte Schritt der Glykolyse ist die reversible Abspaltung eines Moleküls H2O von Glycerinsäure-2-phosphat durch das Enzym Enolase. Es entstehen ein Molekül Wasser und Phosphoenolpyruvat (Phosphoenolbrenztraubensäure).
Der zehnte und letzte Schritt der Glykolyse ist die reversible Übertragung der Phosphatgruppe von Phosphoenolpyruvat auf ADP durch das Enzym Pyruvatkinase. Es entstehen ATP und Pyruvat.
Im Verlauf der Glykolyse entstehen 4 Moleküle Adenosintriphosphat, während nur 2 Moleküle Adenosintriphosphat verbraucht werden, weil nur 1 Molekül Glucose durch den Einsatz von 2 Molekülen Adenosintriphosphat in zwei Schritten aktiviert werden muss, während im weiteren Verlauf 2 Moleküle Glycerinaldehyd-3-phophat entstehen, deren Abbau zu Brenztraubensäure jeweils 2 Moleküle Adenosintriphosphat liefert.
Das Endprodukt der Glykolyse Brenztraubensäure dient unter aeroben Bedingungen als erstes Substrat des Zitronensäurezyklus. Unter anaeroben Bedingungen kann es durch alkoholische Gärung oder durch Milchsäure-Gärung abgebaut werden.
Die Glykolyse muss reguliert werden, damit nicht mehr Adenosintriphosphat gebildet wird, als die Zelle benötigt. Das Enzym Phosphofructokinase eignet sich relativ gut als Schlüsselenzym, weil es das dritte von 10 Enzymen des Stoffwechselweges Glykolyse ist. Die Regulation funktioniert so, dass das Endprodukt Adenosintriphosphat als allosterischer Inhibitor die Aktivität des Schlüsselenzyms Phosphofructokinase durch Reduktion seiner Affinität zum Substrat hemmt, während die Phosphofructokinase durch den allosterischen Aktivator ADP und durch das Substrat Fructose-6-phosphat aktiviert wird.
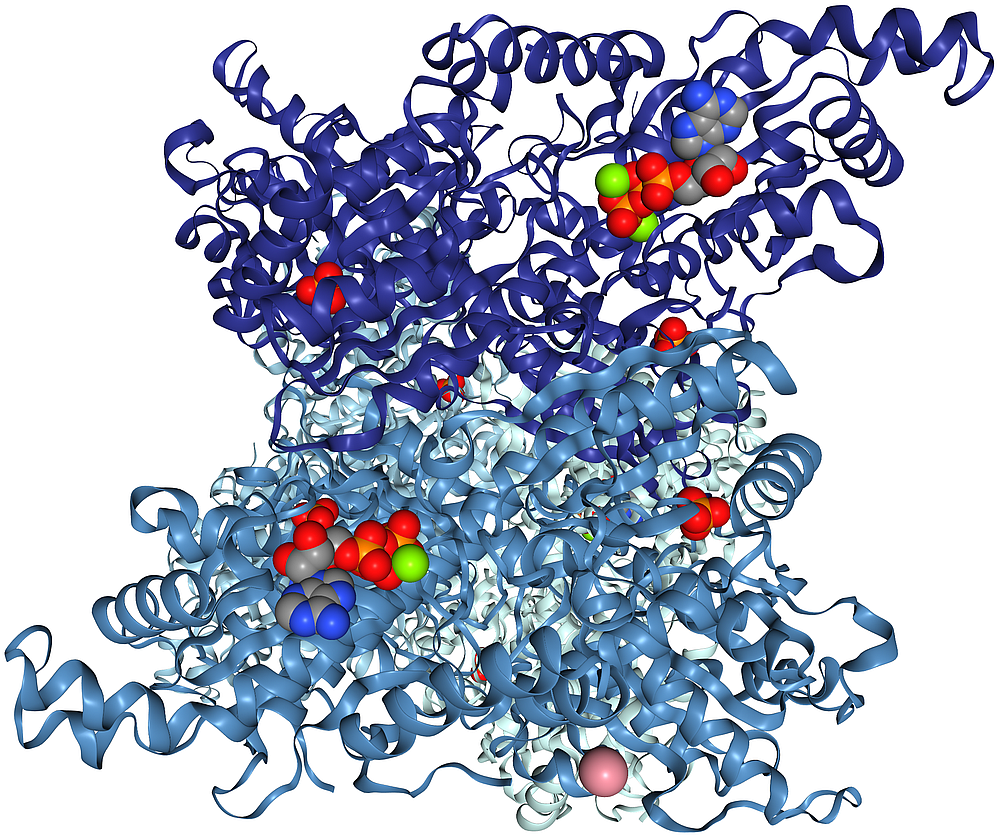
| Schema der Phosphofructosekinase mit gebundenen ATP-Molekülen (4XYJ) | |
|---|---|
 |
|
| Roland Heynkes, CC BY-SA-4.0 (Anklicken des Bildes führt zu einem 3D-Modell.) | |
Oxidative Decarboxylierung und Zitratzyklus - Seiten 122-123
|
|---|
Mit folgendem Link findet Du klausurähnliche Aufgaben zu den Buchseiten 122-123.
Unter aeroben Bedingungen, also bei ausreichender Sauerstoffversorgung, folgt der Glykolyse zunächst ein Abbau der Brenztraubensäure (Pyruvat) durch oxidative Decarboxylierung am Pyruvatdehydrogenase-Enzymkomplex zu Acetyl-CoA, welches dann durch den Zitronensäurezyklus zu CO2 abgebaut wird. Die dabei aus NAD+ und FAD gebildeten reduzierten Cofaktoren NADH und FADH2 werden schließlich in der sogenannten Atmungskette für den Aufbau eines Protonen-Gradienten genutzt, mit dessen Hilfe die ATP-Synthasen als Bestandteile der Atmungskette in den Mitochondrien Adenosintriphosphat als universellen Energieträger der Zelle produzieren.
Im Verlauf der oxidativen Decarboxylierung durch den Pyruvatdehydrogenase-Enzymkomplex wird zunächst vom Pyruvat wird eines seiner 3 C-Atome in Form von CO2 abgespalten. Dabei wird das Kohlenstoff-Atom oxidiert. Wie bei Redoxreaktionen üblich ist die Oxidation des C-Atoms verbunden mit einer Reduktionsreaktion. Und reduziert wird in diesem Fall NAD+ zu NADH. Der vom Pyruvat übrigbleibende Acetyl-Rest wird an das Coenzym A gebunden. Das ist ein Aktivierungsschritt und man nennt das Produkt Acetyl-CoA auch aktivierte Essigsäure.
Das Acetyl-CoA wird in den Zitratzyklus eingebracht. Die Acetylgruppe wird nämlich vom Coenzym A auf Oxalsäure übertragen. Aus der Oxalsäure mit einem Grundgerüst aus 4 C-Atomen wird dadurch eine Kette aus 6 C-Atomen, die man Zitronensäure (protoniert) oder Citrat (deprotoniert) nennt. Beide Namen kann man mit "C" oder "Z" schreiben.
Außer der am Ende wieder heraus kommenden Oxalessigsäure gehen hinein in den Citratzyklus:
1 Molekül Acetyl-CoA + 3 Moleküle H2O + 3 Moleküle NAD+ + je 1 Molekül GDP und Phosphat + 1 Molekül FAD.
Dabei liefert der Zitratzyklus:
1 Molekül Coenzym A + 1 Molekül H2O + 2 Moleküle CO2 + 3 Moleküle NADH+H+ + 1 Molekül GTP + 1 Molekül FADH2.
| Schema des Zitronensäurezyklus |
|---|
|
|
| anonymer Chemiker, Public domain |
Es gibt auffällige Gemeinsamkeiten von Glykolyse und Zitratzyklus:
Weil der Zitratzyklus ein Zyklus ist, muss sein letztes Produkt Oxalessigsäure gleichzeitig sein erstes Substrat sein. Darum muss die anfängliche Verlängerung der Oxalessigsäure durch die Acetylgruppe um zwei C-Atom zu Zitronensäure im Verlauf des Zitratzyklus ausgeglichen werden. Das geschieht in zwei chemischen Reaktionen, bei denen jeweils ein Molekül CO2 vom jeweiligen Substrat abgespalten wird. Dadurch verliert jeweils das Substrat eine Carboxygruppe und damit auch jeweils ein C-Atom.
Man kann im Zitratzyklus 3 verschiedene Reaktionstypen mit H2O als Cosubstrat oder Nebenprodukt unterscheiden:
Bei Bedarf können mit Substraten bzw. Produkten des Zitratzyklus der Aufbau der Aminosäuren Arginin, Asparagin, Asparaginsäure, Glutamin, Histidin, Isoleucin, Methionin, Phenylalanin, Prolin, Threonin, Tyrosin und Valin sowie von Porphyrinen wie Chlorophyll und Hämoglobin beginnen oder deren Abbau enden. Abbau und Aufbau von Fettsäuren und den Aminosäuren Alanin, Cystein, Glycin, Leucin, Serin und Tryptophan sind genau wie Auf- und Abbau von Glucose nur indirekt über Brenztraubensäure bzw. Acetyl-CoA mit dem Zitratzyklus verbunden.
Der Zitratzyklus liefert mit nur einem Molekül GTP pro Umlauf wenig direkt durch die Zelle nutzbare Energie. Die zahlreicher erzeugten reduzierten Cofaktoren sind zwar energiereich, aber diese chemische Energie kann erst durch die Atmungskette zur Produktion des universellen Energieträgers der Zelle Adenosintriphosphat genutzt werden.
Die folgenden Schemata sollen die chemischen Reaktionen des Zitratzyklus veranschaulichen. Dabei habe ich die räumlichen Anordnungen von den dreidimensionalen Darstellungen der offenen chemischen Datenbank PubChem der US-amerikanischen National Institutes of Health (NIH) übernommen und bei den darüber gelegten Buchstaben die relativen Atom-Durchmesser berücksichtigt. Um die Sache übersichtlicher zu machen, zeichne ich alle Strukturen in der protonierten Form, obwohl unter physiologischen Bedingungen im Mitochondrium die Carboxylgruppen deprotoniert sind.
Wenn das Acetyl-CoA aus der oxidativen Decarboxylierung in den Zitratzyklus eingebracht wird, dann hilft die energiereiche Bindung zwischen der Acetylgruppe und dem Coenzym A bei der Übertragung der Acetylgruppe auf die Oxalessigsäure.
Zunächst entfernt das Enzym Citratsynthase eines der drei Protonen aus der Methylgruppe innerhalb der Acetylgruppe. Danach ist das Kohlenstoff-Atom negativ geladen und verdrängt in der Oxalessigsäure die Doppelbindung zwischen dem zweiten C-Atom und dem Sauerstoff-Atom (Ketogruppe). Das danach nur noch einfach gebundene Sauerstoff-Atom ist negativ geladen und bindet das zuvor vom Enzym Citratsynthase aufgenommene Proton. So entsteht das noch am Enzym gebundene Zwischenprodukt Citryl-CoA. Von diesem wird das Coenzym A anschließend durch Hydrolyse abgespalten. Dabei verdrängt der Hydroxygruppe-Rest des Wasser-Moleküls das Schwefel-Atom des Coenzym A. Dabei nimmt dieses Schwefel-Atom das Elektronenpaar seiner Atombindung zum Kohlenstoff-Atom mit und bindet damit das zweite Proton des H2O. So entsteht die Zitronensäure.
Auch die zweite chemische Reaktion des Zitratzyklus erfolgt über ein Zwischenprodukt namens cis-Aconitsäure. Am Enzym Aconitase (Aconitat-Hydratase) entsteht zunächst durch eine Dehydratisierung eine Doppelbindung. Wenn anschließend die Doppelbindung des Zwischenproduktes durch Hydratisierung gelöst wird, dann bindet die Hydroxylgruppe an dem anderen C-Atom der Doppelbindung. Man nennt solche Umlagerungen Isomerisierungen und die Produkte Isomere. Daher der Name Isozitronensäure. Enzyme, die Isomerisierungen katalysieren, heißen Isomerasen.
Die dritte chemische Reaktion des Zitratzyklus ist eine oxidative Decarboxylierung und die erste von vier Redoxreaktionen im Zitratzyklus. Sie erfolgt über ein an das Enzym Isocitratdehydrogenase gebundenes Zwischenprodukt namens Oxalsuccinsäure. Während die Isozitronensäure zu α-Ketoglutarsäure und CO2 oxidiert wird, erfolgt zunächst die Reduktion von NAD+ zu NADH + H+. Anschließend wird ein Molekül CO2 abgespalten.
Auch die vierte chemische Reaktion des Zitratzyklus ist eine oxidative Decarboxylierung und die zweite von vier Redoxreaktionen im Zitratzyklus. Sie wird katalysiert am Enzymkomplex α-Ketoglutarsäure-Dehydrogenase. Während die α-Ketoglutarsäure zu Succinyl-CoA und CO2 oxidiert wird, erfolgt gleichzeitig die Reduktion von NAD+ zu NADH + H+.
Die fünfte chemische Reaktion des Zitratzyklus erfolgt am Enzymkomplex und kann reversibel sein. Zunächst verdrängt anscheinend (laut Wikimedia und dem Lehrbuch: Molecular Biology of the Cell") anorganische Phosphorsäure (bzw. deren deprotoniertes Phosphat) das Coenzym A aus seiner energiereichen chemischen Verbindung mit der Bernsteinsäure. Dann scheint die Phosphatgruppe erst auf einen Histidinrest des Enzyms und schließlich auf Guanidindiphosphat übertragen zu werden. Deshalb scheint weder ein Molekül H2O für die Abspaltung des Coenzym A erforderlich zu sein, noch ein Molekül H2O bei der Verknüpfung von Phosphat und GDP zu GTP frei zu werden. Man nennt diesen Reaktionsmechanismus Substrate-level phosphorylation.
Die sechste chemische Reaktion des Zitratzyklus ist die dritte von vier Redoxreaktionen und erfolgt an dem aus vier Untereinheiten bestehenden Enzymkomplex Succinat-Dehydrogenase mit dem systematischen Namen Succinat:Ubichinon-Oxidoreduktase. Dieser ist gleichzeitig als Komplex II Teil der Atmungskette und befindet sich deshalb als einziges Enzym des Zitratzyklus in den inneren Membranen der Mitochondrien.
Von der auf Deutsch Bernsteinsäure und international in ihrer deprotonierten Form Succinat genannten Succinylsäure werden zwei Wasserstoffatome auf die fest mit dem Enzym verbundene prosthetische Gruppe FAD übertragen, welches dadurch zu FADH2 reduziert wird. Anschließend werden die beiden Protonen vom FADH2 abgespalten und die Elektronen durch den Enzymkomplex und die Membran hindurch auf Ubichinon (Coenzym Q) übertragen.
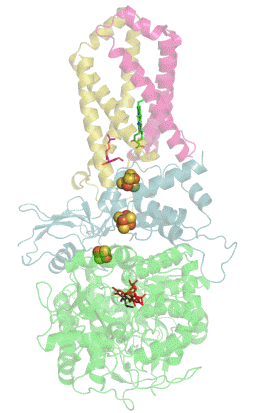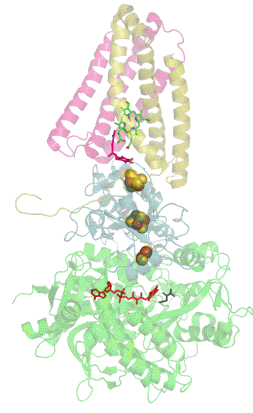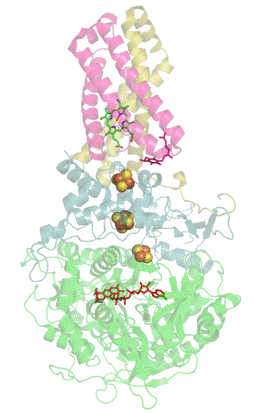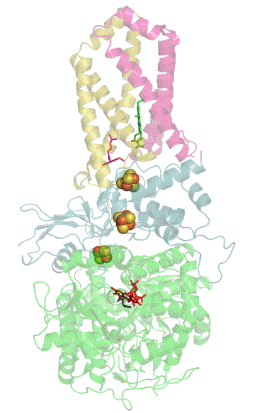
Das folgende animierte gif zeigt den Enzym-Substrat-Komplex und darin unten rot das FAD sowie schwarz das Substrat Succinat.
| Schema des Enzymkomplexes Succinat:Ubichinon-Oxidoreduktase |
|---|
|
| anonym, Public domain |
Die siebte chemische Reaktion des Zitratzyklus ist eine Hydratisierung. Mit einem C-Atom der Doppelbindung verbindet sich eine Hydroxygruppe. Das andere C-Atom der Doppelbindung wird mit dem zweiten Wasserstoffatom abgesättigt. So entsteht aus der international in der deprotonierten Form Fumarat genannten Fumarsäure (englisch: Fumaric acid) die international in der deprotonierten Form L-Malat genannte Äpfelsäure (englisch: Malic acid).
Die achte und letzte chemische Reaktion des Zitratzyklus ist die letzte der vier Redoxreaktionen und wird katalysiert durch das Enzym Malatdehydrogenase. Es überträgt zwei Wasserstoffatome von der Äpfelsäure (englisch: Malic acid, deprotoniert: Malate) auf NAD+. Dabei wird die Äpfelsäure oxidiert zu Oxalessigsäure (englisch: Oxaloacetic acid, deprotoniert: Fumarat). Gleichzeitig wird NAD+ zu NADH+H+ reduziert.
Roland Heynkes, CC BY-NC-SA 4.0